RNA-seq受託解析
RNA-seq解析とは
次世代シーケンサー(NGS)を用いて全転写産物の塩基配列を決定することにより、転写産物量を網羅的に推定できるだけでなく、新規転写産物の探索も可能です。選択したプローブの範囲内でしか変化を検出できないマイクロアレイ法に対して、転写産物を直接シーケンスして発現プロファイルを取得するため、全く予想しなかった発現変化も検出できます。さらに、アレイ法に比べて高発現でも飽和しにくく感度も高いため、ダイナミックレンジが広く高い定量性を持っています。
※受託解析サービスの詳細はこちら
用途
- 既知/新規遺伝子の網羅的発現量推定
- 発現変動遺伝子(DEG)の抽出
- 発現変動遺伝子の機能解析(GO解析*1、GSEA*2など)
※関連する解析サービス
1細胞ごとに網羅的な発現解析を行うシングルセルRNA-seq解析はこちら
このような方に
- Single-cell RNA-seq解析とバルク(通常の)RNA-seq解析の結果を合わせて解釈したい方
- 参考論文と同じような解析を自分のサンプルで実施したい方
- 自分の研究目的に最適な実験デザインの検討から始めたい方
- 共同研究先の対応スピードや、一方向的な情報科学的解析手法にお悩みの方
- 最適なデータ解析手法や適切な統計手法の選択と実施に不安がある方
当社の特徴
- ウェット実験とデータ解析の両分野の経験豊富な専門技術者が直接対応
- 生物学的意義を踏まえたデータ解析(詳細はこちら)
- 論文、学会発表に使用できる各種グラフの作成まで一貫してサポート
- 統計学の専門用語を極力排除した分かり易い説明
- 解析結果の統計学的および生物学的解釈のサポート
※「当社が選ばれる5つの理由」はこちら
解析例
解析例1 マウス新生児肝臓で出生後に見られる遺伝子発現変化
マウス新生児の肝臓RNA-seqデータを用いて、マッピング、発現量推定、発現変動遺伝子(DEG)抽出、GO解析を行いました。
マッピング結果
マッピング結果


チトクロムP450ファミリー遺伝子(Cyp1a2)に対するマッピングデータを図示しました。出生後0日肝臓由来RNAのリードカウント(目的遺伝子に由来するRNAの断片数に相当)を青で、10日肝臓由来RNAの結果を赤で、それぞれ2例ずつ、また遺伝子の構造を緑で表示しました。横軸は染色体上の位置を示しています。同様に全遺伝子にマップされた断片数を数えて正規化し、網羅的に全転写産物の発現量を推定しました。
発現変動遺伝子抽出結果の一例
発現変動遺伝子抽出結果の一例
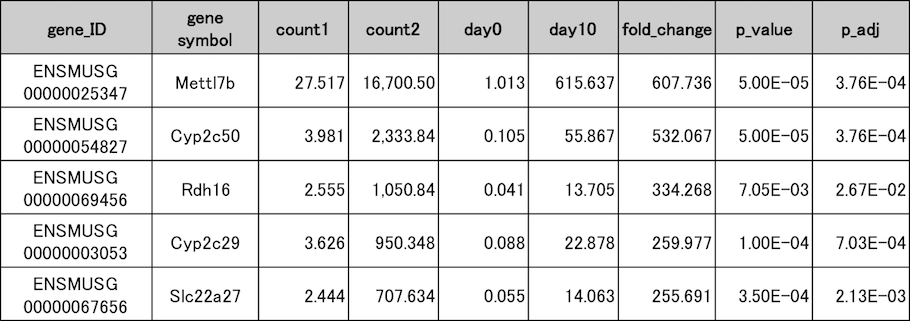

(Mouse newborn liver, Day0 vs Day10, n = 3)
統計検定によりday10で有意に発現量が増加した遺伝子の一部を図示しました。この表はデータ項目を簡略化してあり、実際の納品データとは様式が多少異なります。
発現変動遺伝子に対するGene Ontology(GO)解析
発現変動遺伝子に対するGene Ontology(GO)解析
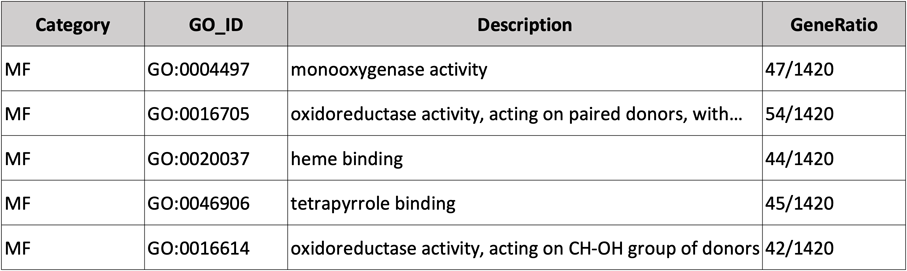

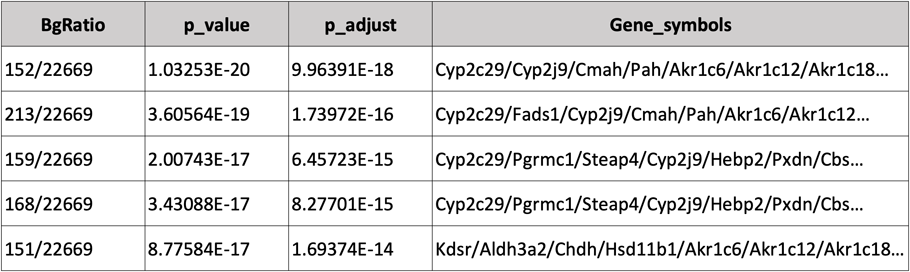

抽出した発現変動遺伝子群を基に、どのような生命現象(機能やパスウェイ)に係る遺伝子が統計的に有意に含まれているか(濃縮しているか)を評価しました。推定された生命現象(GOターム)と統計値、各GOタームに含まれる遺伝子名をリスト表示しています。
ヒートマップによるGO解析結果の可視化
ヒートマップによるGO解析結果の可視化
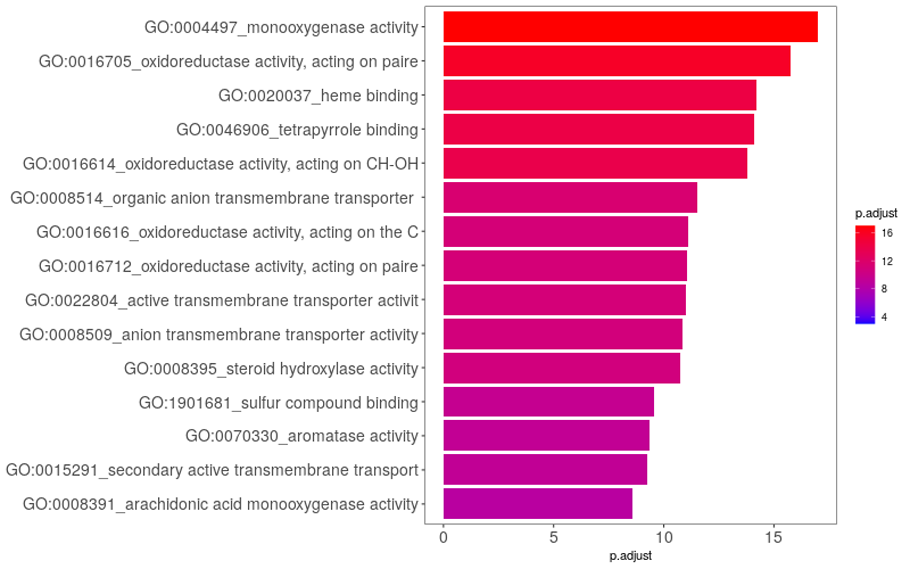

GO解析結果を基に、濃縮されているGOタームを統計的有意性が高い順にヒートマップ表示しました。棒グラフが青色から赤色になるほど統計的有意性が高いことを示しています。
階層性を考慮したGO解析結果の可視化
階層性を考慮したGO解析結果の可視化
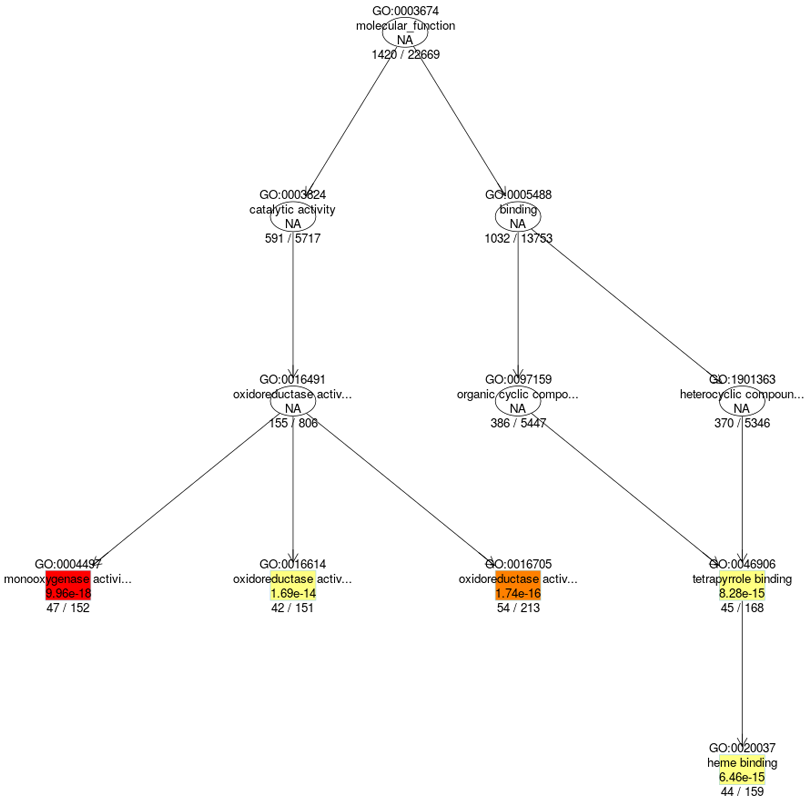

GOタームには階層性があり、広い概念を包括するGOタームにはより狭い概念のGOタームが含まれます。ここでは、そのようなGOターム同士の関係性も考慮し可視化しました。背景色が赤色のGOタームは統計的な有意性が高く、オレンジ>黄色>白色の順に統計的有意性が低くなります。図の下側、すなわち狭い概念のGOタームで濃縮が見られた場合には、より特異的な生物学的応答が起こったと推定されます。
解析の結果、Monooxygenase activityに関するGOタームを持つ遺伝子が有意に高い割合で含まれることが分かりました。 新生児期にはmonooxygenaseの一種であるチトクロムP450の種類や発現量が大きく変化すると言われており、そのような変化が検出された可能性が考えられます。RNA-seq解析からはこの様に、細胞集団全体で起こった特徴的な変化を事前予測なしに抽出することが可能です。
しかし、試料中に少数しか存在しない細胞で特徴的な変化が起こるような場合には、感度的には検出可能であっても「網羅的に解析する」ことは困難なため、その様な解析には、1細胞ごとに発現プロファイルを取得するSingle Cell RNA-seq解析法が用いられます。 Single Cell RNA-seq解析サービスについてはこちらをご覧ください。
解析例2 幹細胞から分化誘導した心房細胞の薬剤処理による遺伝子発現変化
幹細胞の利用方法の一つとして、多能性幹細胞を分化誘導した細胞を用いた創薬スクリーニングの高効率化が期待されています。ibrutinibは有用な経口白血病治療薬ですが、心房細動を増加させる事が知られています。ヒト多能性幹細胞から誘導した心房心筋細胞をibrutinib処理し、RNA-seq解析を実施したデータを使用して、 ibrutinib処理による心房心筋細胞のRNA発現変化を解析しました。
遺伝子発現量推定結果
遺伝子発現量推定結果
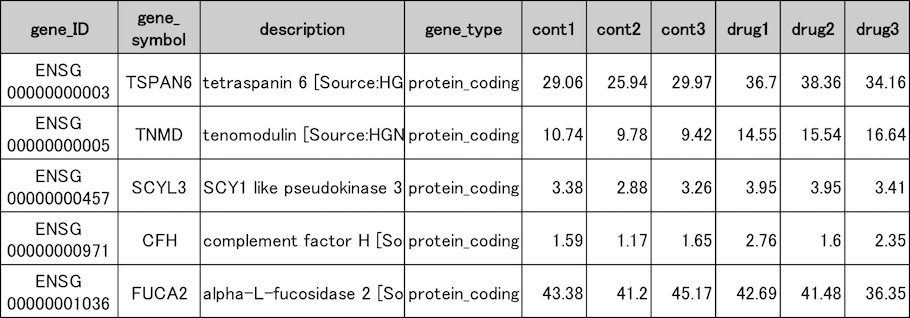

薬剤未処理の(cont1〜3)心房心筋細胞と、薬剤処理した細胞(drug1〜3)の遺伝子発現量推定結果の一部を示しました。
発現変動遺伝子抽出結果の一例
発現変動遺伝子抽出結果の一例
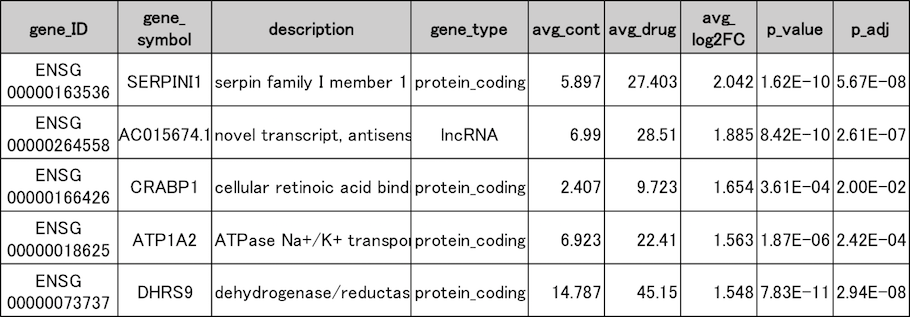

薬剤未処理群(cont1〜3)と、処理群(drug1〜3)の発現変動遺伝子の一部を示しました。
ヒートマップによる発現変動遺伝子の可視化
ヒートマップによる発現変動遺伝子の可視化
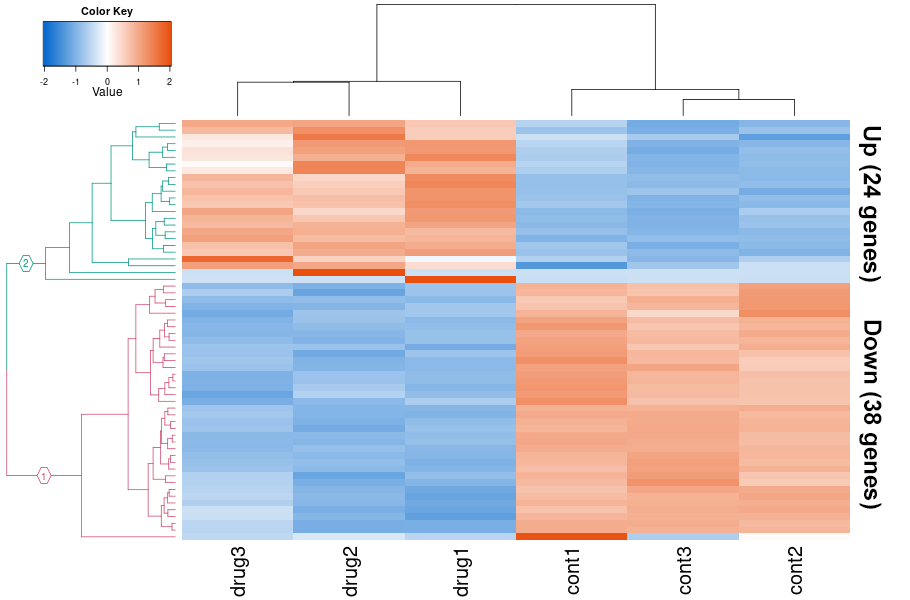

発現変動遺伝子の発現変化をヒートマップで一覧表示しました。各サンプルの発現量をZ-scoreで標準化し、発現量が多い遺伝子を赤色、少ない遺伝子を青色、中間を白色で表示しました。図の縦軸は遺伝子、横軸はサンプルを表します。
ボルカノプロットによる発現変動遺伝子の可視化
ボルカノプロットによる発現変動遺伝子の可視化
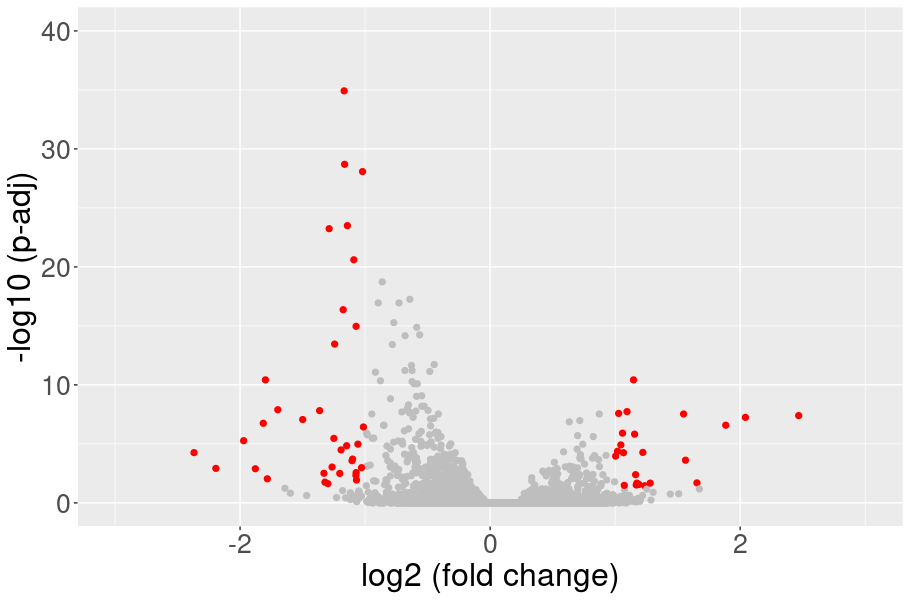

ボルカノプロットで発現変動比と統計的有意差を一覧表示しました。各点は遺伝子を表しています。発現変動比と調整済みp値によって分類し色分け表示しました。
GSEA(Gene Set Enrichment Analysis)
GSEA(Gene Set Enrichment Analysis)
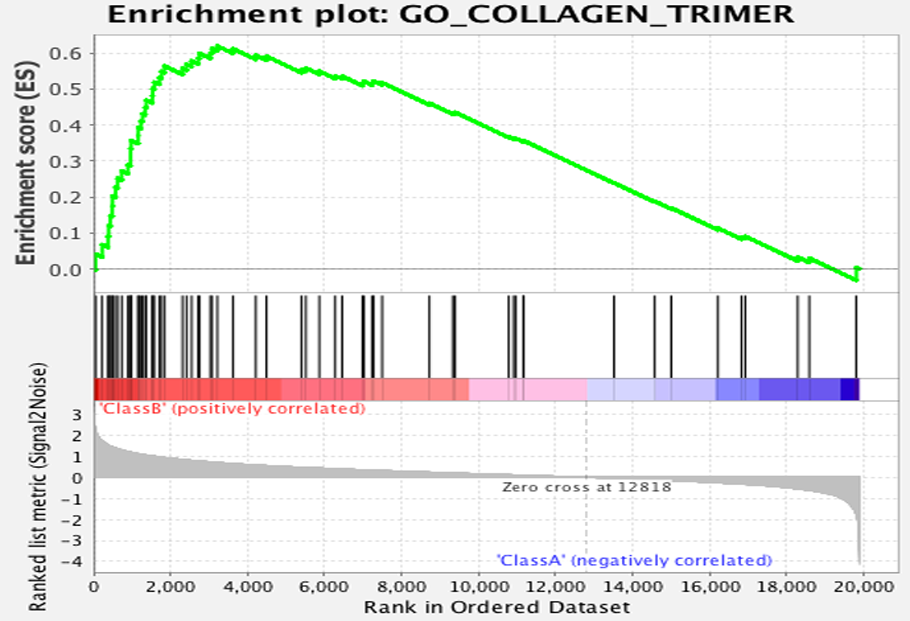

薬剤処理によって発現が増加・減少した遺伝子が特定の遺伝子セットに濃縮しているか、GSEAを用いて解析しました。
解析例3 がん浸潤T細胞サブタイプの発現変動遺伝子抽出とパスウェイ解析
大腸がん患者から採取したがん浸潤CD8+ T細胞と末梢血中CD8+ T細胞それぞれを、FACSによりソーティングしたサブタイプのRNA-seqデータを用いて、各サブタイプの特徴を解析しました。
既知の細胞表面マーカーによるCD8+ T細胞の分類
既知の細胞表面マーカーによるCD8+ T細胞の分類
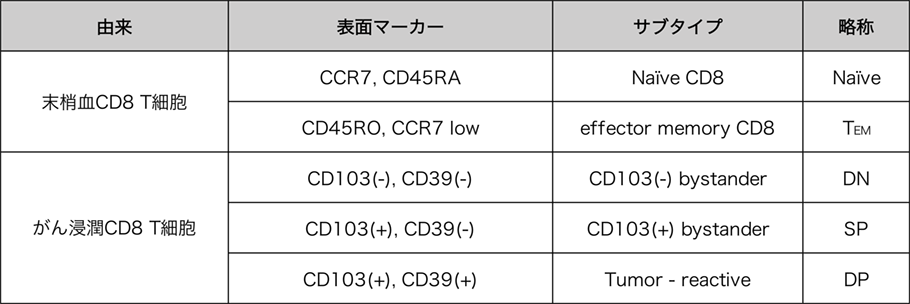

各CD8+ T細胞サブタイプに特徴的な遺伝子発現(ヒートマップ)
各CD8+ T細胞サブタイプに特徴的な遺伝子発現(ヒートマップ)
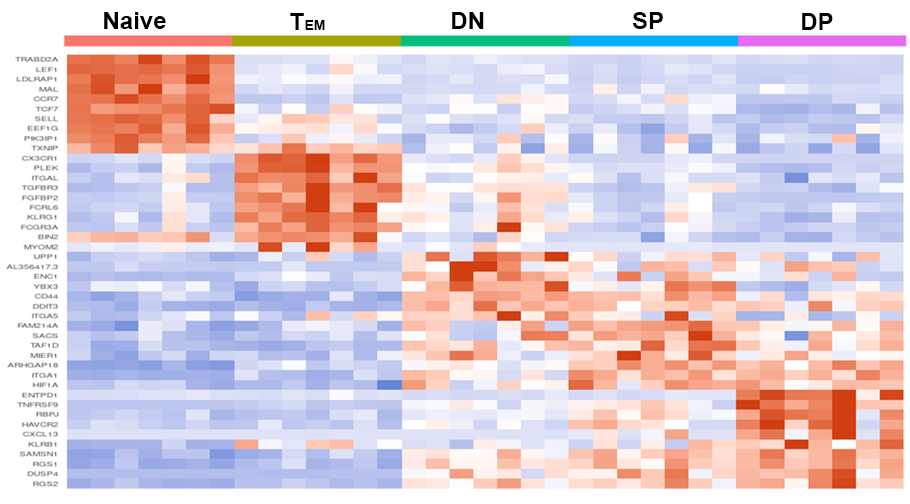

各CD8+ T細胞サブタイプに特徴的な遺伝子の発現をヒートマップで一覧表示しました。FACSによりソーティングされた集団ごとの特徴が網羅的に抽出されました。
PCAおよび相関分析による各検体間の類似性評価
PCAおよび相関分析による各検体間の類似性評価
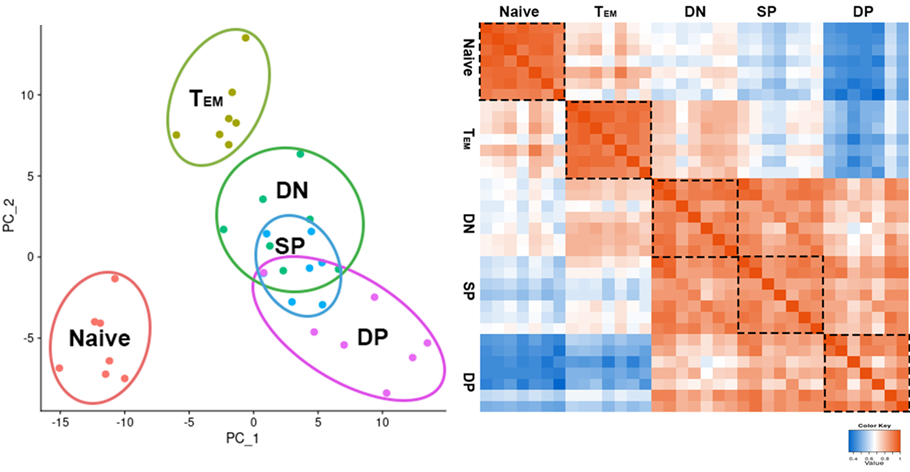

PCA(主成分分析、左図)および、検体間の相関係数のヒートマップ表示(右図)により各検体間の類似性を評価しました。
がん浸潤CD8+ T細胞のサブタイプごとの発現変動遺伝子のベン図
がん浸潤CD8+ T細胞のサブタイプごとの発現変動遺伝子のベン図
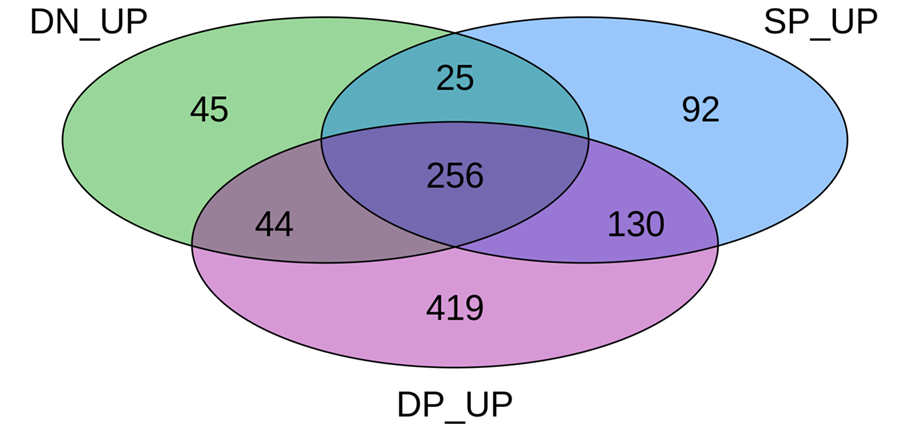

3種類のがん浸潤CD8+ T細胞サブタイプとTEM細胞の発現プロファイルを比較して、それぞれのがん浸潤CD8+ T細胞サブタイプで発現量が増加した発現変動遺伝子を抽出し、その集合関係をベン図で表示しました。以降の解析結果は、DP(がん応答性サブタイプ)について示しました。
ボルカノプロットによる発現変動遺伝子の可視化
ボルカノプロットによる発現変動遺伝子の可視化
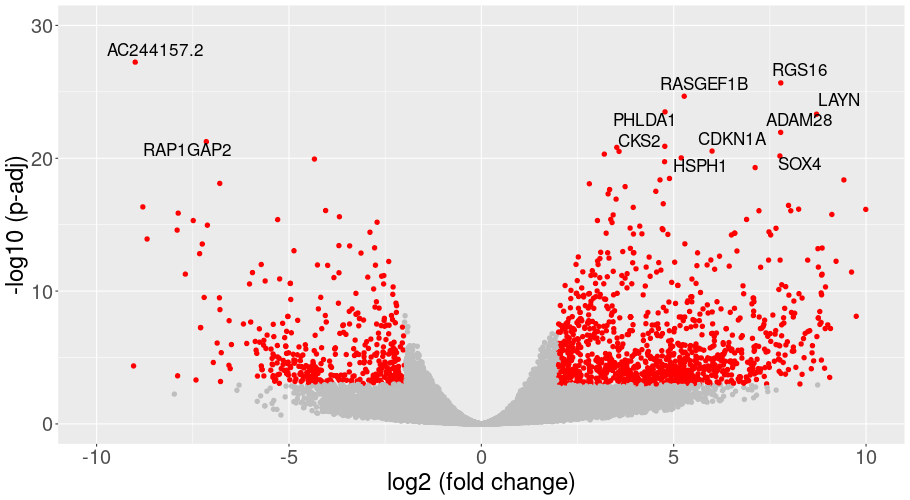

DPとTEMの間で発現が変化した遺伝子を、発現変動比と統計的有意差を用いたボルカノプロットで一覧表示しました。各点は遺伝子を表しています。
DPの発現変動遺伝子のパスウェイ解析
DPの発現変動遺伝子のパスウェイ解析
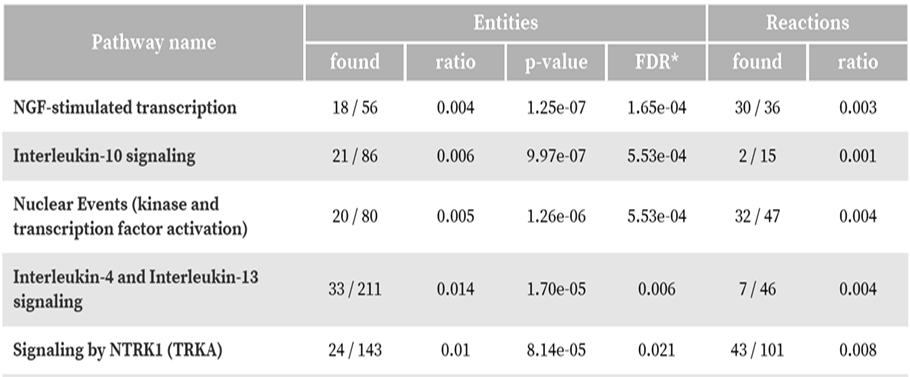

非常に多数の発現変動遺伝子が見出された場合、どのような応答が起こったかをパスウェイ解析によって俯瞰することができます。TEMと比較してDPで発現が増加した発現変動遺伝子が、統計的有意に濃縮しているパスウェイを抽出しました。
Interleukin-10 signaling pathwayの模式図
Interleukin-10 signaling pathwayの模式図
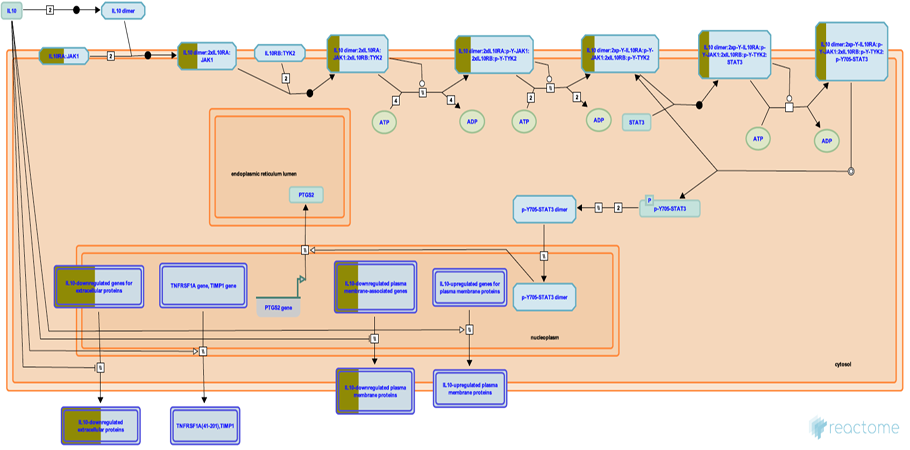

抽出したパスウェイの内、Interleukin-10 signaling pathwayの詳細を表示しました。
Interleukin-10 signaling pathway上での各遺伝の発現変動比
Interleukin-10 signaling pathway上での各遺伝の発現変動比
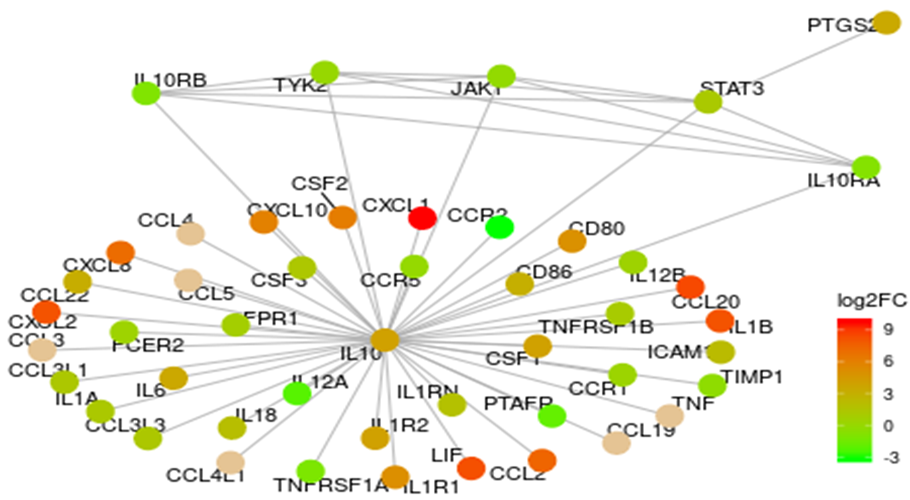

Interleukin-10 signaling pathway に含まれる遺伝子の発現変動比を図示しました。DPで発現が増加した遺伝子を赤、減少した遺伝子を緑で表示しました。
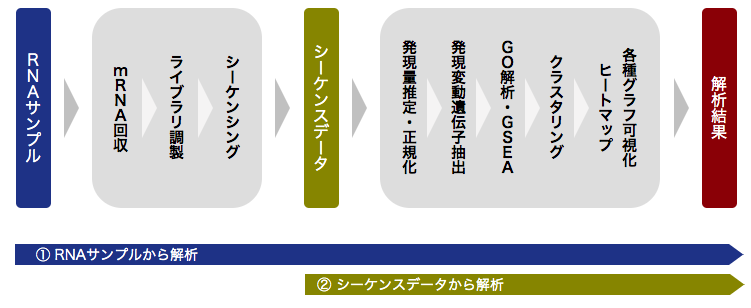
解析フロー
RNAサンプル
mRNA回収
ライブラリ調製
シーケンシング
シーケンスデータ
発現量推定・正規化
発現変動遺伝子抽出
GO解析・GSEA
クラスタリング
ヒートマップ
各種グラフ可視化
解析結果
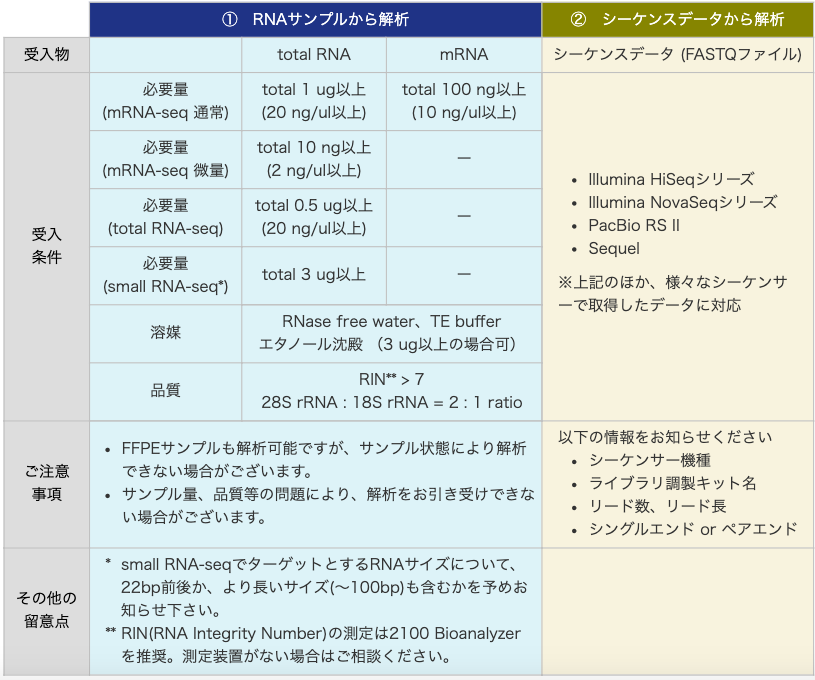
受入物
| ① RNAサンプルから解析 | ② シーケンスデータから解析 | |||
|---|---|---|---|---|
| 受入物 | total RNA | mRNA | シーケンスデータ (FASTQファイル) | |
| 受入 条件 |
mRNA-seq 通常量タイプ |
total 1 ug以上 (20 ng/ul以上) |
total 100 ng以上 (10 ng/ul以上) |
※上記のほか、様々なシーケンサーで取得したデータに対応
|
| mRNA-seq 微量タイプ |
total 10 ng以上 (2 ng/ul以上) |
ー | ||
| total RNA-seq | total 0.5 ug以上 (20 ng/ul以上) |
ー | ||
| small RNA-seq* | total 3 ug以上 |
ー | ||
| 溶媒 | RNase free water エタノール沈殿 (3 ug以上の場合可) |
|||
| 品質 | RIN** > 7 28S rRNA : 18S rRNA = 2 : 1 ratio |
|||
| ご注意 事項 |
|
以下の情報をお知らせください
|
||
| その他の 留意点 |
|
|||
解析内容
- mRNAシーケンシング(通常量・微量タイプ)
-
- 網羅的なmRNAの塩基配列決定
- mRNAの網羅的な発現量推定、発現差解析に最適(別途データ解析)
-
【 解析内容 】
- 検体の受入検査(RNA量、濃度、純度、分解の有無)
- ライブラリ調製
- シーケンシング
-
【 解析条件 】
- 検体受入検査 : Agilent Bioanalyzer / TapeStation
- シーケンサー : Illumina Novaseq 6000 / X
- シーケンス : 100bp、ペアエンド、4,000万リード(4Gb/検体)
- Total RNAシーケンシング
-
- 網羅的なmRNA、lncRNA等のnoncoding RNAの塩基配列決定
- 分解が進んだtotal RNAからのmRNAの塩基配列決定
- mRNA、lncRNA等のnoncoding RNAの発現量推定、発現差解析に最適(別途データ解析)
-
【 解析内容 】
- 検体の受入検査(RNA量、濃度、純度、分解の有無)
- rRNA除去
- ライブラリ調製
- シーケンシング
-
【 解析条件 】
- 検体受入検査 : Agilent Bioanalyzer / TapeStation
- シーケンサー : Illumina Novaseq 6000 / X
- シーケンス : 100bp、ペアエンド、4,000万リード(4Gb/検体)
- データ解析(スタンダード1)
-
- 発現量推定が目的で、安価に解析したい場合にお勧めです。
- k-mer countingにより発現量を推定
- 既知遺伝子、転写産物の発現量推定
- マッピングの可視化が不要な場合に最適
- 他の解析でBAMファイルを使用しない場合に推奨
- mRNAおよびTotal RNAシーケンシングのデータに対応
- 参照配列はトランスクリプトームを使用
-
【 解析内容 】
- データ受入検査(データ量、シーケンス品質、アダプタ配列の有無等)
- 不要な配列のトリミング
- k-mer counting
- 発現量推定・正規化
- 発現変動遺伝子抽出(DEG抽出、発現比較解析)
- データ解析(スタンダード2)
-
- 発現量推定が目的で、マッピングの可視化が必要な場合にお勧めです。
- 参照ゲノム配列にマッピングし発現量を推定
- 既知遺伝子、転写産物の発現量推定
- 他の解析でBAMファイルを使用する場合に推奨
- mRNAおよびTotal RNAシーケンシングのデータに対応
- 参照配列はゲノムを使用
-
【 解析内容 】
- データ受入検査(データ量、シーケンス品質、アダプタ配列の有無等)
- 不要な配列のトリミング
- マッピング
- 発現量推定・正規化
- 発現変動遺伝子抽出(DEG抽出、発現比較解析)
※上記の他、GO解析、GSEA、パスウェイ解析や各種グラフの作成も承っています。
価格・納期
ご要望に合わせて実験デザインをご提案し、御見積致しますのでこちらよりお問い合わせ下さい。
※全解析(ウェット+ドライ)のご依頼の場合は、6検体から受け入れています。
※ウェットのみのご依頼の場合は、12検体から受け入れています。
ご注意事項
受入物を品質検査した結果、解析をお引き受けできない場合があります。
お問い合わせ
こちらよりお問い合わせください。
専門技術者が原則24時間以内にご連絡します。(土日祝日は除く)
参考文献
Sumedha S. Gunewardena et al. “Deciphering the Developmental Dynamics of the Mouse Liver Transcriptome.” PLoS One. 2015 Oct 23;10(10) e0141220. doi: 10.1371/journal.pone.0141220.
Shafaattalab, S. et al. “Ibrutinib Displays Atrial-Specific Toxicity in Human Stem Cell-Derived Cardiomyocytes.” Stem Cell Reports 12, 996–1006 (2019). doi: 10.1016/j.stemcr.2019.03.011.
Yang, R. et al. “Distinct epigenetic features of tumor-reactive CD8+ T cells in colorectal cancer patients revealed by genome-wide DNA methylation analysis.” Genome Biology 21, (2020). doi:10.1186/s13059-019-1921-y
*1 Gene Ontology
*2 Gene Set Enrichment Analysis
